Хлорид натрия
 Хлорид натрия встречается в природе в морской воде, которая содержит приблизительно 2,7 % соли в виде каменной соли в больших залежах мощностью около 1000 метров. Такие залежи встречаются около Величии в Галиции и в Северогерманской.
Хлорид натрия встречается в природе в морской воде, которая содержит приблизительно 2,7 % соли в виде каменной соли в больших залежах мощностью около 1000 метров. Такие залежи встречаются около Величии в Галиции и в Северогерманской.
Северогерманские соляные залежи возникли при высыхании большого внутреннего моря, просторы которого в первобытные времена начинались от Урала и тянулись в глубину теперешней Франции и теперешнего Северного моря, которое было тогда отрезано от Атлантического океана. Оно простиралось на юг почти до теперешней долины Дуная. При очень жарком в то время климате, особенно летом, происходило быстрое испарение воды. Это приводило к выделению растворенных в морской воде солей в соответствии с их концентрациями, растворимостью и разницей температур воды летом и зимой. Прежде всего выпадал не растворимый в воде карбонат кальция, который лежит поэтому в виде «цехштейновского известняка» под собственно солевыми залежами. После этого образовывались другие соли, причем летом именно ангидрит, гипс и полигалит, а зимой каменная соль. Наконец происходило осаждение калийной соли. Участки моря, которые высохли, покрывались песком. Позднее верхние слои, содержащие соли калия, были снова смыты.
Поваренную соль получают такими тремя способами: 1) из морской воды испарением в так называемых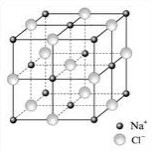 «соляных садках», а в условиях холодного климата — вымораживанием; 2) горнопромышленной разработкой каменной соли; 3) растворением каменной соли под землей и выпариваниям полученного рассола.
«соляных садках», а в условиях холодного климата — вымораживанием; 2) горнопромышленной разработкой каменной соли; 3) растворением каменной соли под землей и выпариваниям полученного рассола.
Как правило, в технике каменную соль добывают путем горнопромышленной разработки в виде побочного продукта при получении калийных солей. Самостоятельная разработка каменной соли выгодна лишь при содержании в ней 98-99 % хлорида натрия. Если соль более загрязненная, то ее не добывают, а оставляют в шахте, где она применяется для заполнения выработанных проходов в пластах солей калия.
Каменная соль главным образом в своем составе имеет сульфаты магния и кальция. Определенную ее очистку достигают ручным отбором кусков гипса и ангидрита после грубого измельчения соли. Дальнейшая очистка осуществляется обработкой или плавлением более чистыми рассолами.
Приготовление пищевой соли, к которой в смысле чистоты предъявляются наибольшие требования, производят главным образом выпариванием естественных или искусственно полученных (путем растворения под землей) водных солевых растворов, так называемых рассолов.
 Полученная таким путем соль называется выварочной солью. Перед выпариванием, которое ведут в плоских противнях, рассолы доводят до насыщения. Ранее это производили испарением на воздухе. С этой целью рассол заставляли стекать по стене, сложенной из связок хвороста (градирня). Теперь в большинстве случаев в рассоле растворяют до насыщения добытую каменную соль.
Полученная таким путем соль называется выварочной солью. Перед выпариванием, которое ведут в плоских противнях, рассолы доводят до насыщения. Ранее это производили испарением на воздухе. С этой целью рассол заставляли стекать по стене, сложенной из связок хвороста (градирня). Теперь в большинстве случаев в рассоле растворяют до насыщения добытую каменную соль.
Перед выпариванием рассол очищают добавлением хлорида кальция (для удаления сульфатов) и едкой извести (для удаления магния). Выделяющейся гидроксид магния, действуя как адсорбирующее вещество, увлекает одновременно собой и органические примеси.
Чистый хлорид натрия не гигроскопичен. Известное увлажнение поваренной соли на влажном воздухе объясняется содержанием в ней примесей. Хлорид натрия кристаллизуется в виде бесцветных правильных кубов удельного веса 2.17. При температуре плавления 801 °С он уже заметно летуч, однако в меньшей степени, чем хлорид калия. Плотность пара соответствует формуле NаС1.
Поваренная соль необходима живому организму, особенно при растительном характере пищи. Поэтому ее добавляют в корма для скота. Ее применяют при консервировании мяса и рыбы (соление), В технике хлористый натрий является исходным сырьем для получения почти всех других соединений натрия.
Каменная соль является основным исходным материалом при производстве соляной кислоты и сульфата, получения соды, хлора и едкого натра. Кроме того, она служит для многих других промышленных и промысловых целей, например для высаливания мыла и органических красителей; для «хлорирующего обжига» в некоторых металлургических процессах; и кожевенном производстве для соления кож; для глазурования глиняных изделий, для ускорения таяния снега и приготовления охладительных смесей и т. д.
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.