Получение концентрированной азотной кислоты
Для проведения некоторых интересных опытов необходима концентрированная азотная кислота. Такую кислоту можно получить в лаборатории из нитрата натрия и концентрированной серной кислоты.
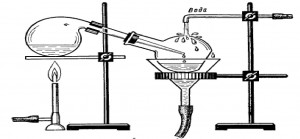
Составьте прибор, как показано на рис.
Вместо реторты иногда принимают круглодонную колбу. Ее следует закрыть пробкой, сделанной из асбестовой массы (влажной). Пробку старательно заливают менделеевской замазкой, чтобы она не пропускала газов.
Нитрата натрия и концентрированной серной кислоты для реакции берут столько, чтобы образовалось 30 г азотной кислоты. Серной кислоты надо брать на 30-40 % больше теоретически вычисленной количества, считая, что в условиях эксперимента образуется гидросульфат натрия:
NaNO3 + H2SO4 = NaHSO4 + HNO3
Нагрейте реторту (колбу) на песчаной бане или на асбестовой сетке. Сначала немного, а потом сильнее. В приемнике собирается почти бесцветная жидкость – концентрированная азотная кислота. Приемник все время охлаждайте, поместив его в кристаллизатор с холодной водой.
Отзывов (12) на «Получение концентрированной азотной кислоты»
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.
22 Окт 2011 в 14:45
А что такое-менделеевская замазка? Что-то никогда не слышал о такой.
22 Окт 2011 в 15:23
Классные опыты у вас!
22 Окт 2011 в 19:00
Классные И такие опасненькие
22 Окт 2011 в 19:18
Очень занимательно))
22 Окт 2011 в 21:59
Я в школе очень любила неорганическую химию! А вот органическую — чего не понимаю, того не понимаю, да и учить такие длинные цепочки связей было мне не по нраву. Жаль, что в мои школьные годы у нас не была интернета, а то может быть и я химию полюбила бы и знала бы на отлично!
22 Окт 2011 в 22:15
это очень специфическая статья. Но, видимо, для тех, кто этим занимается, очень полезна.
22 Окт 2011 в 23:07
Много из нее взрывчатых веществ можно сделать. А в мирных целях — платы травить, но тут разбавить нужно слегка.
22 Окт 2011 в 23:14
Как всегда читаю с удовольствием. Материалы короткие, насыщенные и оригинальные.
21 Дек 2011 в 12:46
ребята помоги пожалуйста задачу решить)))))из 34 г. нитрата натрия при действии концентрированной серной кислотой получили 22,7г азотной кислоты. вычислите массовую долю выхода азотной кислоты.! буду очень благодарен!!!!!
22 Дек 2011 в 11:56
выручайте кто может)))) очень на зачет надо!!!№ 1) при взаимодействии раствора серной к-ты массой 16г. с избытком раствора хлорида бария выделяется осадок массой 35,7г. Вычислитее массовую долю продукта.
—
№ 2) Смешали 150г раствора и 200г 5% раствора соляной к-ты.Определите массовую долю соляной к-ты в полученном растворе
—
№ 3) Напишите молекулярные, полные и сокращённые ионные уравнения реакций между растворами:
А) нитратом цинк и сульфидом калия
б)сульфатом магния и гидрооксидом натрия
—
№ 4) составьте ур-ния реакций, протекающих в водных растворах, в молекулярной,ионной и скоращённой ионной формах:
1)между нитритом серебра и соляной к-той
2)между гидрооксидом натрия и сульфатом меди(2 валентность).
22 Дек 2011 в 11:59
задачу 2 не надо решать!!!!
22 Дек 2011 в 15:44
помогите кто нибудь!!!!!! очень буду благодарен тому кто поможет!!!!!!!!!!!!