Определение Э. д. с. гальванических элементов
В стаканы наливают на 1/2 высоты 1 М раствора хлорида магния, сульфата цинка, хлорида никеля, нитрата свинца, сульфата меди, Аргентум нитрата и погружают в соответствии электроды: магниевый, цинковый, никелевый, медный, серебряный.
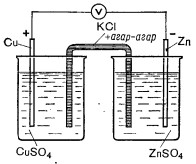
Соединяют попарно растворы в стаканах с помощью агар-агаровой сифона (рис.), электроды погружают в растворы и присоединяют их к вольтметру.
Рис. Схема медно-цинкового гальванического элемента
Определяют Э. д. с. гальванических элементов. Сравнивают экспериментально определенную Э. д. с. гальванических элементов с вычисленным значениям Э. д. с. по величинам нормальных электродных потенциалов:
Мg | Мg2+= ‒ 2,36 В;
Zn | Zn2+ = ‒ 0,76 В;
Ni | Ni2+ = ‒ 0,25 В;
Рb | Рb2+ = ‒ 0,13 В;
Сu | Сu2+ = + 0,34 В;
Аg | Аg+ = + 0,80 В.
Рекомендуется сравнить результаты опыта с рядом напряжений.
Реактивы и оборудование: хлорид магния МgС12, сульфат цинка ZnSO4, хлорид никеля NiCl2, нитрат свинца Pb(NO3)2, сульфат меди СuSO4, Аргентум нитрата АgNO3; 7 химических стаканов емкостью по 200 мл, агар-агарный сифон, электроды-пластинки металлов одинакового размера, вольтметр.
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.