Электролитическое восстановление нитробензола до анилина
Опыт проводят в приборе, который изображен на рис. В основе этого опыта лежит реакция восстановления нитробензола атомарным водородом:
С6Н5∙NО2, + 6Н → С6Н5∙NH2 + 2Н2O.
В химический стакан вставляют пористый глиняный стакан, который закрепляют на штативе. В пористый стакан, который выполняет роль диафрагмы, содержащие анод — пластинку свинца. Вторую свинцовую пластинку сгибают и помещают в электролизер, как показано на рис.
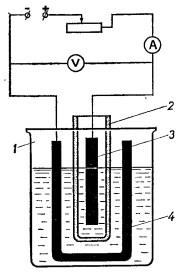
Рис. Прибор для восстановления нитробензола до анилина:
1 — электролизер (химический стакан), 2 — пористый глиняный стакан,
3-анод (свинцовая пластинка). 4 — катод (согнутая свинцовая пластинка)
Готовят раствор: 5 г нитробензола добавляют к 40 мл этилового спирта, в который добавляют 35 мл 25-процентного раствора серной кислоты. Этим раствором заполняют внешнее пространство электролизера. Глиняный пористый стакан заполняют до того же уровня 15-процентным раствором серной кислоты. Электролиз проводят в течение 15 мин, пропуская электрический ток напряжением 20 В, силой 3-4 А.
На катоде во внешнем пространстве происходит процесс восстановления водорода.
Н2SO4 → 2Н+ + 3SО42-,
Н+ + e— = Н°, 2Н° = Н2.
Атомарный водород ‒ сильный восстановитель ‒ восстанавливает нитробензол в анилина.
Анилин обнаруживают, добавляя несколько капель катодного раствора в концентрированный раствор хлорной извести (фильтрованный на холоде). При этом появляется интенсивное фиолетовое окрашивание, тогда как исходный раствор этого окраски не дает.
Реактивы и оборудование: нитробензол С6Н5NO2, этиловый спирт С2Н5ОН, серная кислота Н2SO4, хлорная известь Са(С1O)2; высокий химический стакан емкостью 300 мл, глиняный пористый стакан, свинцовые электроды, провода, источник постоянного тока
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.