Металлы в молекулярной клешне
Есть немало соединений, структура каких напоминает клешни рака или краба, которые «мертвой хваткой» держат добычу. Такие интересные соединения называются хелатами (от греческого «хел?» — клешня). А образуются они так: молекула вещества своими двумя, тремя, а то и большим количеством атомов прочно сцепляется с атомом металла. Итак, молекула, образует с металлом клешнеобразный комплекс, который должен быть полидентатными, т.е. «многозубым». Попав в «плен» к такой молекулы, металлический атом-пленник перестраивает свою электронную оболочку. В свою очередь он влияет и на молекулу. Вследствие этого одни электронные орбитали комплекса сжимаются, другие расширяются. Молекула-клешня посылает свои электроны на орбитали атома металла. Такая связь называют донорно-акцепторной. В свою очередь атом-пленник посылает свои электроны на орбитали молекулы-клешни. Это так называемый обратный донорно-акцепторный, или дативный связок.
Следовательно, и молекула «хищник» и атом «добыча» существенно изменяются, приспосабливаясь к сосуществованию. Благодаря этому в хелатах появляются особенности, которых не было в его составных частей к комплексообразованию: меняются окраска, растворимость, термические, электрические, магнитные и другие свойства.
Если добавить раствор какой-нибудь аминокислоты, например глицина, до светло-голубого осадка дигидроксиду меди, последний легко растворяется. При этом образуется темно-синий раствор аминоацетату меди. И раствор этой соли в отличие от растворов карбоната меди СuCО3, нитрата меди Сu(NО3)2, ацетата меди Сu(СН3СОО)2 тока не проводит. Следовательно, в растворе свободные катионы и анионы отсутствуют, а следовательно, структуре аминоацетату меди не может соответствовать следующая формула:
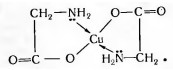
На самом же каждый остаток аминокислоты — бидентатный двузубый. Два аминоацетатных аниона захватывают своими четырьмя «клешнями» (четырьмя «зубами») атом меди:
Подобные соединения очень прочные. Многие из них (бетадикетонаты металлов, основной гексаацетат бериллия и др.) даже перегоняются, не разлагаются.
Осадки бес-диметилглиоксимоникелю, а также палладия выпадают из щелочных растворов, тогда как аналогичный хелат железа (II), кобальта, меди и других металлов растворимый. Это широко используют для количественного определения никеля в железных метеоритах, в земных сплавах: нержавеющей стали, монель-металле, нойзильбери, нихрома и др., а также в различных рудах и минералах.
Окраска зеленых листьев растений, красной крови человека и голубой крови осьминога, или спрута, зависит от хелатов: хлорофилла, гемоглобина и гемоцианин.
Хелаты играют важную роль не только в природе. С их помощью разделяют и выделяют в чистом виде редкоземельные и урановые металлы, добывают чистые реакторные материалы, проводят химические анализы, «смягчают» воду. Хелаты помогают значительно дольше сохранять ракетное топливо, сливочное масло, мясо, консервированную кровь. В последнее время хелаты некоторых переходных металлов применяются в качестве рабочего тела лазера.
Отзывов (5) на «Металлы в молекулярной клешне»
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.
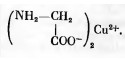
30 Окт 2011 в 15:48
Спасибо за урок с наглядными схемами.
30 Окт 2011 в 15:59
Интересно конечно, но я долек от химии, многие термины не понял.
30 Окт 2011 в 18:46
Смотри-ка ты! Прямо как в живой, вернее в большой природе. Лианы тоже клешнями захватывают растение, по которому вьются. и получается очень интересный … коллективчик. )))
30 Окт 2011 в 19:31
Наша земля тоже пленник у солнца! Аналогии: очень совпадают
30 Окт 2011 в 23:59
Так живенько про донорно-акцепторную связь! Интересная статья. Спасибо.